
摘要:心源性休克两个主要病因是急性心肌梗死和急性失代偿性心力衰竭(Acutely Decompensated Heart Failure,ADHF) 。影响预后的最大因素是早期临床评估、明确病因、及时应用药物治疗或个体化循环机械支持。血流动力学监测有助于对心源性休克进行临床类型分析,借助Swan-Ganz导管等监测工具,有利于指导治疗选择。设立专门的休克团队至关重要,有助于尽快决策最佳治疗策略,降低死亡率。
心源性休克:心源性休克主要指由于心脏泵功能障碍导致器官灌注不足的状态。临床试验或指南中对心源性休克的定义多种多样,通常基于低血压(收缩压低于90 mmHg 或平均动脉压低于65 mmHg),同时存在器官低灌注的迹象,例如少尿、乳酸增加和精神状态改变。心脏指数小于2.2 mL/min/m2和肺楔压大于15 mmHg等血流动力学参数,有时与心脏功率输出(Cardiac Power Output,CPO)等其他指标一起用于定义心源性休克。必须强调的是,即使在没有低血压的情况下,心源性休克也可能出现低灌注(由于外周阻力增加的代偿机制)。与仅有低血压而没有低灌注迹象的情况相比,这种表型具有更高的死亡风险。
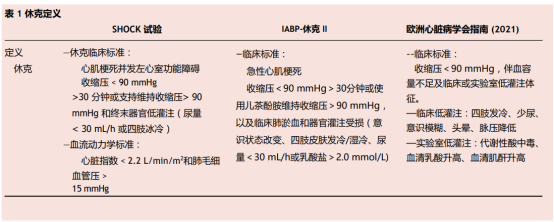
心源性休克的分型:2019 年,心血管造影和介入学会(SCAI)提出了心源性休克严重程度的分期,将患者分为五个阶段,很好地概括了该综合征的动态和进展性质。大量后续研究证明了SCAI分期与院内死亡率之间的相关性,也强调了心肌梗死患者同一阶段的预后与心力衰竭加重相比更差。

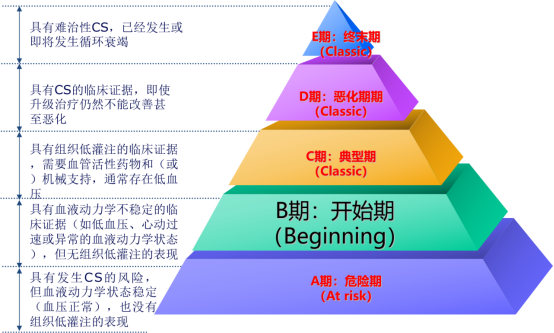
休克的分型和快速识别。(J Clin Med. 2023 Apr 1; 12(7):2643.)(2023中国急性心力衰竭指南)
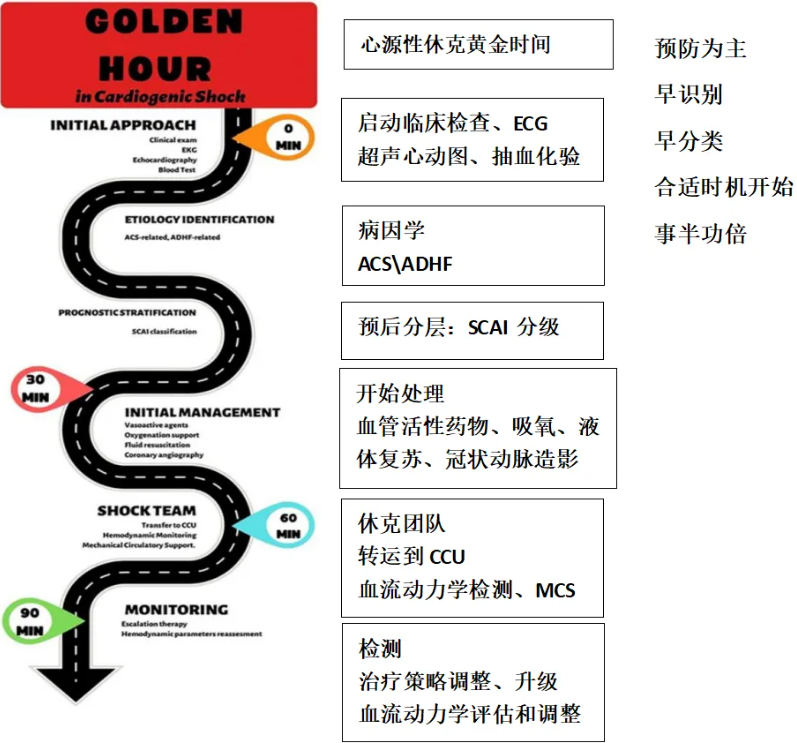
心源性休克早期识别和危险分层:事半功倍( Well Begun Is Half Done.)
(J Clin Med. 2023 Apr 1; 12(7):2643.; Eur Heart J Suppl. 2024 Apr 17;26(Suppl 1):i78-i83.)
心源性休克属于一种时间依赖性的危重症,从首次临床接触开始就需要制定针对性治疗方案,其早期分类与初步处理的黄金时间窗被定义为"黄金一小时"。
心源性休克的治疗
1、心源性休克的治疗基于两个基本基石
治疗潜在病因(例如急性梗塞时的心肌血运重建)和通过使用血管活性药物和机械支持装置改善灌注和氧合的支持疗法。
2、液体抗休克治疗
对于血流动力学依赖于前负荷的非充血性患者,应考虑通过推注生理盐水或乳酸林格氏液(250 毫升,15-10 分钟内输注)进行液体管理。
3、机械通气
应在患者到达时根据临床表现和血气分析数据评估患者的通气支持类型(无创通气或有创机械通气),同时考虑到正压通气后负荷降低带来的血流动力学益处。
4、血管活性药物
血管活性药物(正性肌力药、血管加压药和扩张药)与院内发病率和死亡率的增加有关,其机制如下:增加心脏做功,增加氧消耗和诱导心律失常。因此,应根据患者的血流动力学需求进行个体化给药,在尽可能短的时间内使用最少的足够剂量,并考虑到当前的血流动力学特征。欧洲心脏病学会指南建议使用(Class IIb/B类)去甲肾上腺素作为一线血管加压药。
在OPTIMACC(比较肾上腺素和去甲肾上腺素在心源性休克中的疗效和耐受性的研究)对比研究中,即使使用非常高的剂量,肾上腺素也表现出更高的乳酸性酸中毒发生率、更高的心率值(更大的氧消耗)和死亡率。可以考虑辅助使用正性肌力药物来改善CO 和器官灌注(Class IIb/C 类)。
左西孟旦、米力农和多巴酚丁胺之间没有显著差异,在肾功能不全的情况下优先选择多巴酚丁胺,而一般情况下优先选择左西孟旦,这也在最近的Cochrane 荟萃分析中得到了强调。
加压素可以在难治性低血压或右心失代偿的情况下发挥作用,因为它选择性地作用于体循环,而不影响肺血管阻力。同样,在右心室功能障碍普遍存在的情况下,多巴酚丁胺、左西孟旦或米力农/依诺昔酮是首选,尤其是在接受β受体阻滞剂治疗的患者中。
5、紧急血运重建
对于急性心肌梗死引起的心源性休克,建议进行紧急血运重建,1999年SHOCK试验(我们是否应该紧急重建闭塞的冠状动脉以治疗心源性休克)的证据支持了这一建议,该试验表明,在心源性休克组中,6个月死亡率较低与药物治疗组相比,更早接受血运重建治疗(50%比63%,P=0.027)。
6、机械循环支持
出现极度心源性休克、病情恶化或使用两种血管活性药物后血流动力学不稳定的患者,可从个体化的机械循环支持中受益(Class IIa/C类建议)。左心室支持的选择包括主动脉内球囊泵(IABP)和微轴流泵(Impella CP、Impella 5-5.5)。右心室辅助系统包括Impella RP、Tandem-Heart right atrium–pulmonary artery devices和Protek Duo。
最后,为了改善严重双心室功能障碍和伴随的急性呼吸窘迫综合征病例的器官灌注,可以使用V-A ECMO。由于Intra-Aortic Balloon Pump in Cardiogenic Shock(IABP-SHOCK)试验显示缺乏生存获益,IABP的使用随着时间的推移而减少。值得注意的是,86% 的患者在血管成形术后植入了该装置。目前,它被认为对于非心肌梗死引起的难治性休克患者(ClassIIb/C 类)或存在机械并发症的心肌梗死引起的心源性休克患者,作为通向更高级支持的桥梁(ClassIIa/C 类)。
尽管Impella看起来很有前景,但关于其对死亡率有益作用的数据很少。在2017年发表的IMPRESS in Severe Shock研究中,急性心梗合并心源性休克患者按照1:1的比例随机分配至Impella CP组和IABP组,组间基线水平无统计学差异。结果显示Impella CP组和IABP组患者的30天全因死亡率分别为46%和50%,6个月死亡率均为50%,两组间无统计学差异。类似地,ECMO可以改善心肺复苏期间的血流动力学稳定性,并增加左心室的后负荷,因此当与允许左心室“卸载”的设备(例如IABP、Impella、隔膜造口术和混合回路配置)结合使用时是合理的。然而,最近发布的 ECLS-SHOCK(梗死相关心源性休克的体外生命支持)和 ECMO-CM(心源性休克治疗中的体外膜氧合)试验提供的数据并不令人满意,当然由于样本量小且这些试验的患者症状普遍比较严重导致研究也可能存在局限性。
Impella和ECMO等设备需要将大口径鞘管插入主要血管,并伴有很高的并发症风险,包括穿刺部位并发症和出血。在心源性休克中,文献报道的Impella置入后严重出血的发生率为8.5%至31%不等;因此,应在专家团队的监督下对选定的患者使用该设备(植入前评估血管通路)。
文献中关于在心源性休克早期阶段,甚至在施用正性肌力药物或心肌血运重建之前使用上述机械支持(单心室和双心室类型)的数据很少。
“Detroit cardiogenic shock initiative(Detroit心源性休克倡议)”是一项单组、多中心试点研究,旨在评估在一小群心源性休克患者(n = 41)中早期应用机械支持循环的可行性,与“历史”对照队列相比,在死亡率方面取得了良好的结果(85% 比 51%,P < 0.001),并且在手术后CPO指数增加了67%。
Altshock-2 研究(急性失代偿性心力衰竭并发心源性休克的早期IABP)正在意大利进行,这是一项前瞻性、随机、多中心、开放标签试验,采用盲法结果评估,其中200名因ADHF导致心源性休克的患者将随机分配到早期植入IABP 或血管活性治疗组。
在心源性休克患者的管理中,需早期实施基于证据的针对循环系统的机械支持,这种“door to support”(门到支持)的及时干预策略可以提高生存率,预防心源性休克恶性循环的有害影响。
休克团队和网络
心源性休克的表现多种多样、严重程度和潜在原因、缺乏对所提出治疗(如机械支持)的有力证据以及个性化治疗的需求,使决策更加复杂,并且需要多学科团队。
“中心辐射”模型的引入已被证明对“现实生活”环境中的救护结果产生积极影响。“中心”医院配备一支多学科团队,由介入心脏病专家、急诊专家、心脏外科医生和晚期心力衰竭专家组成。“辐射”医院包括配备导管实验室但缺乏先进循环支持的中心或未配备导管实验室的医院,两者都需要高级胸痛中心的支持。枢纽中心应配备休克团队,为辐射中心提供足够的信息,包括升级治疗的必要性、高级支持的必要性、选择合适支持的正确导管插入术、充分的围手术期管理和监测以及可能的支持。
关于急性心肌梗死和ADHF所致心源性休克的区域性方案的实施,既可行又与生存率提高相关。Papolos A. 等人进行的一项多中心观察性研究对有无休克团队的重症监护病房进行了比较,发现休克团队的存在对重症监护病房的影响与更广泛地使用深静脉导管插入术和减少血管活性药物的给药有关。拥有休克团队的中心使用较少的机械支持,但更经常使用高级支持(例如Impella和ECMO)。
在这个模型中,急诊室起着战略作用,因为它参与了心源性休克患者的早期识别、初步稳定以及分诊到适当的治疗类型。
结论
心源性休克是一种复杂的综合征,死亡率很高。它的管理应该包括尽可能标准化的协议,并包括一个由多学科专家组成的团队。在所有要考虑的变量中,很明显及时的临床架构在激活警报方面是多么重要,这可以转化为相当于心肌梗死“黄金时间”的管理策略。需要进一步的研究以确凿的证据支持“门到支持”援助干预循环的原则,以预防心源性休克恶性循环的有害影响。需要进一步开展研究,以确凿证据支持"门到支持"循环辅助干预原则,以预防心源性休克恶性循环带来的致命性后果。
参考文献:
1.Rathod KS, Koganti S, Iqbal MB, Jain AK, Kalra SS, Astroulakis Z et al. Contemporary trends in cardiogenic shock: incidence, intra-aortic balloon pump utilisation and outcomes from the London Heart Attack group. Eur Heart J Acute Cardiovasc Care 2018;7:16–27.
2.Shah M, Patnaik S, Patel B, Ram P, Garg L, Agarwal M et al. Trends in mechanical circulatory support use and hospital mortality among patients with acute myocardial infarction and non-infarction related cardiogenic shock in the United States. Clin Res Cardiol 2018;107: 287–303.
3.Jentzer JC, Burstein B, Van Diepen S, Murphy J, Holmes DR, Bell MR et al. Deffning shock and preshock for mortality risk stratiffcation in cardiac intensive care unit patients. Circ Heart Fail 2021;14:e007678.
4.Kapur NK, Kanwar M, Sinha SS, Thayer KL, Garan AR, Hernandez-Montfort J et al. Criteria for deffning stages of cardiogenic shock severity. J Am Coll Cardiol 2022;80:185–198.
5.Mebazaa A, Tolppanen H, Mueller C, Lassus J, DiSomma S, Baksyte G et al. Acute heart failure and cardiogenic shock: a multidisciplinary practical guidance. Intensive Care Med 2016;42:147–163.
6.McDonagh TA, Metra M, Adamo M, Gardner RS, Baumbach A, Böhm M et al. 2021 ESC guidelines for the diagnosis and treatment of acute and chronic heart failure: developed by the task force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC). With the special contribution of the Heart Failure Association (HFA) of the ESC. Eur J Heart Fail 2022;24:4–131. Figure 1 Modiffed from Polyzogopoulou E., Bezati S., Karamasis G., Boultadakis A., Parissis J. Early Recognition and Risk Stratiffcation in Cardiogenic Shock: Well Begun Is Half Done. J Clin Med. 2023 Apr 1; 12(7):2643. i82 M . M a r i n i et al.
7.Fuernau G, Desch S, de Waha-Thiele S, Eitel I, Neumann F-J, Hennersdorf M et al. Arterial lactate in cardiogenic shock: prognostic value of clearance versus single values. JACC Cardiovasc Interv 2020;13:2208–2216.
8.Tehrani BN, Truesdell AG, Psotka MA, Rosner C, Singh R, Sinha SS et al. A standardized and comprehensive approach to the management of cardiogenic shock. JACC Heart Fail 2020;8:879–891.
9.Fincke R, Hochman JS, Lowe AM, Menon V, Slater JN, Webb JG et al. Cardiac power is the strongest hemodynamic correlate of mortality in cardiogenic shock: a report from the SHOCK trial registry. J Am Coll Cardiol 2004;44:340–348.
10.Uhlig K, Efremov L, Tongers J, Frantz S, Mikolajczyk R, Sedding D et al. Inotropic agents and vasodilator strategies for the treatment of cardiogenic shock or low cardiac output syndrome. Cochrane Database Syst Rev 2020;11:CD009669.
11.Menon V, Slater JN, White HD, Sleeper LA, Cocke T, Hochman JS. Acute myocardial infarction complicated by systemic hypoperfusion without hypotension: report of the SHOCK trial registry. Am J Med 2000;108: 374–380.
12.Thiele H, Zeymer U, Neumann F-J, Ferenc M, Olbrich H-G, Hausleiter J et al. Intraaortic balloon support for myocardial infarction with cardiogenic shock. N Eng J Med 2012;367:1287–1206.
13.Basir MB, Schreiber T, Dixon S, Alaswad K, Patel K, Almany S et al. Feasibility of early mechanical circulatory support in acute myocardial infarction complicated by cardiogenic shock: the Detroit cardiogenic shock initiative. Catheter Cardiovasc Interv 2018;91: 454–461.
14.Lu DY, Adelsheimer A, Chan K, Yeo I, Krishnan U, Karas MG et al. Impact of hospital transfer to hubs on outcomes of cardiogenic shock in the real world. Eur J Heart Fail 2021;23:1297–1937.
作者简介:

叶发民主任简介:中共党员,临床硕士,阜外华中心血管病医院(国家心血管病中心华中分中心,河南省人民医院心脏中心)CCU主任医师,中国医师协会心脏重症专业委员会器官功能支持学组副组长,河南省研究型医院学会心脏重症专业委员会副主任委员,河南省呼吸与危重症学会重症医学分会常务委员,河南省医学会心血管病学分会第一届心血管急重症学组委员,河南省医师协会心血管内科医师分会第三届委员会委员,河南省医师协会心血管内科医师分会首届心脏重症学组委员,河南省医学会重症医学专科分会委员,河南省医学会重症医学专科分会第二届青年委员。长期从事临床重症诊治工作,有丰富临床工作经验,擅长于心脏重症临床诊治,在重症感染救治、重症营养支持治疗等,尤其在有创气道建立、机械通气、CRRT、IABP、ECMO、Impella等应用于重症患者救治经验丰富。国内外发表医学论文20余篇,出版专著2部。
供稿:叶发民
编辑:吴莹

诚挚感谢您对“河南心脏 Henan Heart”的关注与支持。
